Généralités
S. Le Roux …. authors to be listed here !
L’architecture dendritique est probablement l’une des topologies les plus répandues dans la nature. Elle est observée, non seulement dans des systèmes non biologiques (cristaux de neige, érosion fractale), mais également au sein du monde biologique (neurones, systèmes vasculaires, arbres) où les dimensions varient du mètre (arbres), au millimètre (champignons), jusqu’au micromètre (neurones).
Le terme dendrimère (du grec « dendron » = arbre et « meros » = partie) a été évoqué pour la première fois dans les années 1940 par Flory [1] Cependant, il faudra attendre la fin des années 70 et les travaux de Vögtle [2] et surtout de Tomalia [3] pour réussir la première synthèse chimique d’un dendrimère régulier. Caractérisées par une structure tridimensionnelle, ces macromolécules de taille nanoscopique sont apparentées à des polymères hyperbranchés, où les monomères branchés sont associés selon un processus arborescent autour d’un cœur central multivalent. Elles adoptent, en général, une forme globulaire. La construction arborescente s’effectue par la répétition d’une même séquence de réactions jusqu’à l’obtention, à la fin de chaque cycle réactionnel, d’une nouvelle génération et d’un nombre croissant de branches identiques. Précisons que les polymères hyperbranchés, dont l’architecture moléculaire est irrégulière, sont obtenus à la suite de la polymérisation de monomères branchés multifonctionnels ABn suivant un processus non-itératif (Figure 1) [4].
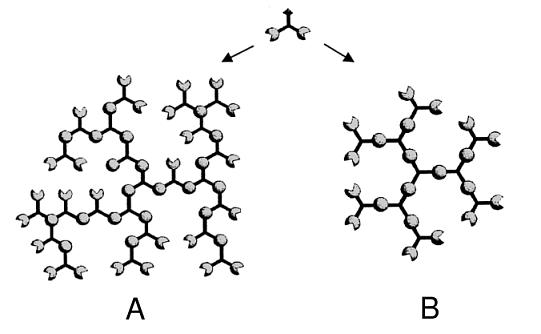
Figure 1 : Organisation tridimensionnelle d’un monomère en polymère hyperbranché (A) et en dendrimère (B)
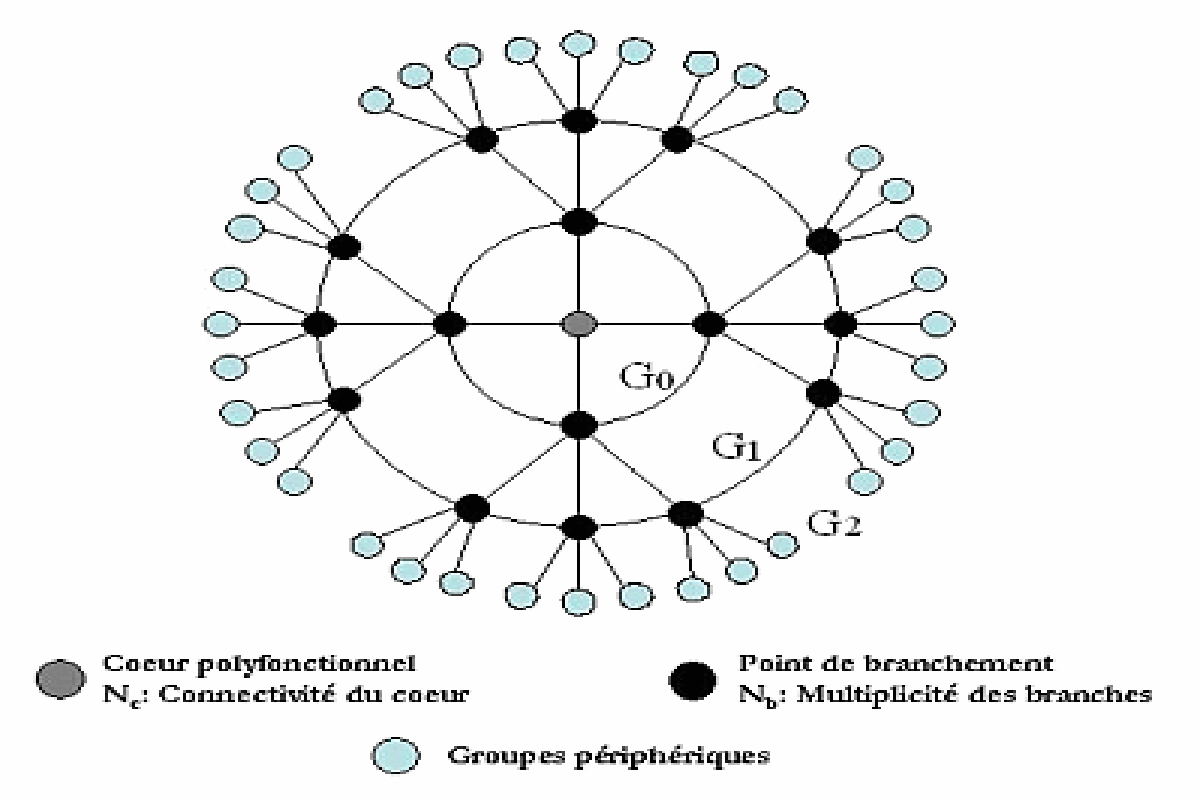
Les dendrimères sont caractérisés par trois régions bien spécifiques : le cœur central, les branches dendritiques et la périphérie. Leur structure est schématiquement représentée dans la Figure 2. Le nombre de branches dendritiques connectées au cœur central polyvalent est défini par la connectivité du cœur Nc, et chaque unité de branchement de multiplicité Nb, caractérise une génération, G, du dendrimère.
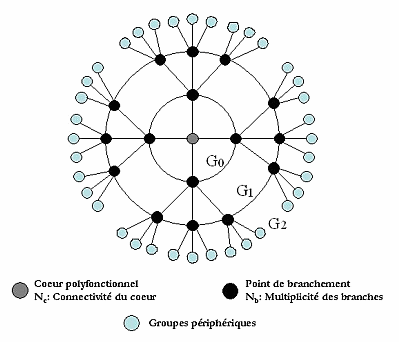
Figure 2 : Représentation schématique de la structure d’un dendrimère.
Tandis que les polymères hyperbranchés sont polydisperses, les dendrimères, du fait de leurs méthodes de synthèse, sont en général monodisperses. Cependant, la croissance des dendrimères n’est pas infinie et est limitée par des phénomènes de congestion stérique décrits par de Gennes [5].
Diverses propriétés physiques sont propres aux dendrimères. Une des caractéristiques les plus originales concerne l’évolution de la viscosité η avec la taille [6]. Celle-ci croît linéairement avec l’augmentation de la génération jusqu’à un certain seuil à partir duquel η diminue considérablement (Figure 3). En outre, la solubilité de ces macromolécules diffère sensiblement des polymères linéaires analogues. Par exemple, la solubilité d’un dendrimère de type polyéther dans du THF est cinquante fois plus grande que celle du polymère linéaire.
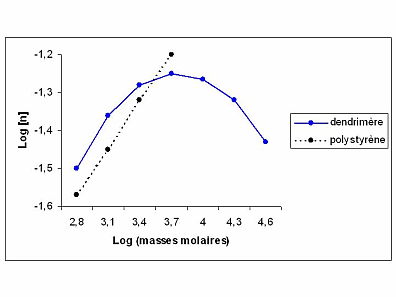
Figure 3 : Représentation graphique logarithmique de la viscosité η en fonction de la masse molaire pour un dendrimère et pour un polystyrène.
D’autres propriétés, comme la variation de la température de transition vitreuse au sein d’une série de dendrimères, sont plus similaires à ce qui a déjà été observé avec des polymères linéaires [7].
Les possibilités d’application offertes par les dendrimères sont particulièrement nombreuses et sont liées à leur topologie originale composée de trois régions bien spécifiques : le cœur, les branches formant la matrice dendritique et la périphérie constituée d’une multitude de groupes fonctionnels (Figure 4).
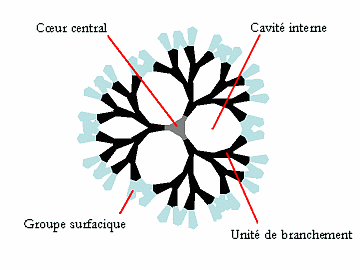
Figure 4 : Morphologie dendritique unique.
Les dendrimères Cristaux Liquides
Le caractère amphipathique des mésogènes est prépondérant dans la formation de cristaux liquides. Ainsi, l’incompatibilité de mélange entre des chaînes aliphatiques apolaires et des parties polaires ou aromatiques favorise une microségrégation à l’origine de la formation des mésophases. L’originalité structurale des dendrimères suscite, depuis peu, un réel intérêt dans le champ d’investigation des cristaux liquides. Les propriétés mésomorphes des dendrimères (type de phase, températures de transition et stabilité thermodynamique) sont fortement dépendantes de la balance enthalpie/entropie (compétition entre énergie d’interaction de type van der Waals, donc d’un gain enthalpique, et la tendance du cœur dendritique à l’isotropisation, donc au désordre) et de la taille des différentes parties les constituant. On peut distinguer plusieurs familles de dendrimères mésomorphes, caractérisés par une architecture bien spécifique.
Les dendrimères à groupements périphériques
S. Le Roux …
Caractérisés par des dendrimères en étoile constitués d’un corps dendritique souple et en périphérie d’unités totalement incompatibles avec ce cœur, les dendrimères à chaînes périphériques composent la famille de dendrimères mésomorphes chimiquement la plus étudiée. La microségrégation, provoquée par l’incompatibilité de mélange entre les unités périphériques et la matrice dendritique ainsi que par les interactions de type van der Waals entres les groupes anisotropes, est à l’origine de la formation de mésophases (Figure 5). Ces unités peuvent être, indifféremment, des groupes mésogènes, pro-mésogènes et non mésogènes (pas d’anisotropie). De nombreux travaux montrant la formation de mésophases lamellaires, cubiques et colonnaires ont été réalisés sur ces dendrimères. Ainsi, Lattermann [8] a montré que le greffage de molécules de 3-4,bis(dodécyloxy)benzoyl en périphérie d’un squelette dendritique du type (polypropylène-imine) induit une anisotropie de structure aboutissant à la formation de mésophases colonnaires (Figure 6 A). En revanche, l’utilisation de mésogènes du type cyanobiphényle a permis au groupe de Meijer [9], de générer des mésophases lamellaires (Figure 6 B).

Figure 5 : Structure schématique d’un dendrimère à chaînes périphériques.
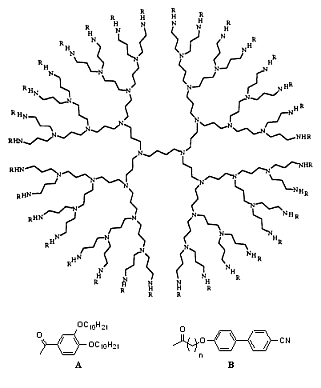
Figure 6 : Dendrimère du type poly(propylène) avec deux types de groupes mésogènes périphériques.
Dendrimères mésomorphes supramoléculaires ou dendromésogènes
S. Le Roux …
Percec et ses collaborateurs [10] ont développé, depuis une quinzaine d’années, une famille de dendrimères bien spécifique, constituée de groupes benzyliques connectés entre eux par des jonctions éthers, les groupes périphériques étant des chaînes alkoxy. Suivant le degré de substitution des unités répétitives, les dendrimères obtenus adoptent une forme soit conique ou en coin, soit sphérique, s’auto-organisant en entités supramoléculaires caractérisées respectivement par des structures colonnaires et cubiques. Notons que la taille du dendrimère et donc la génération joue un rôle important sur la conformation.
Dendrimères a chaînes principales
S. Le Roux …
Parmi les différentes familles de dendrimères cristaux liquides, une seule n’a pas été mentionnée; il s’agit des dendrimères dits à chaînes principales pour lesquels, des mésogènes sont incorporés au sein de la matrice dendritique constituant les points de branchement du dendrimère et sont séparés par des chaînes flexibles aliphatiques (Figure 7).
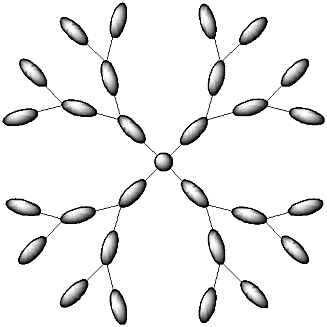
Figure 7 : Structure schématique d’un dendrimère à chaîne principale
Les groupes anisotropes étant présents à tous les niveaux de l’architecture dendritique, le dendrimère est forcé d’adopter une conformation régulière et bien définie, et il en résulte la formation de mésophases. [1] P.J. Flory, J. Am. Chem. Soc., 63, 3083 (1941); P.J. Flory, J. Am. Chem. Soc., 63, 3091 (1941); P.J. Flory, J. Am. Chem. Soc., 63, 3096 (1941).
[2] E. Buhleier, W. Wehner, F. Vögtle, Synthesis, 155 (1978).
[3] D.A. Tomalia, H. Baker, J. Dewald, M. Hall, G. Kallos, S. Martin, J. Roeck, J. Ryder, P. Smith, Polym. J., 17, 117 (1985).
[4] P.J. Flory, Principles of polymer chemistry, chap. 9, Cornell University Press, Ithaca, New York (1952); A. Hult, M. Johansson, E. Malmström, Adv. Poylm. Sci., 143, 1 (1999).
[5] P.G. de Gennes, H.J. Hervet, J. Physique-Lett., 44, 351 (1983).
[6] J.M.J. Fréchet, C.J. Hawker, K.L. Wooley, Pure Appl. Chem., A31, 1627 (1994).
[7] J.MJ. Fréchet, Science, 1994, 263, 1710
[8] J.H. Cameron, A. Facher, G. Lattermann, S. Diele, Adv. Mater., 9, 398 (1997).
[9] M.W.P.L. Baars, S.H.M. Söntjens, H. M. Fischer, H.W.I. Peerlings, E.W. Meijer, Chem. Eur. J., 4, 2456 (1998)
[10] G. Ungar, V. Percec, M.N. holerca, G. Johansson, J.A. Heck, Chem. Eur. J., 6, 1258 (2000); V. Percec, W. Cho, G. Ungar, J. Am. Chem. Soc., 122, 10273 (2000); V. Percec, W-D. Cho, G. Ungar, D.J.P. Yeardley, J. Am. Chem. Soc., 123, 1302 (2001); G. Ungar, Y. Liu, X. Zeng, V. Percec, W. Cho, Science, 299, 1208 (2003).